La colina è stata identificata come un nutriente nei primi anni ’30, quando è stato dimostrato come la lecitina (una fonte di colina) fosse in grado di prevenire l’insorgere della patologia del fegato grasso sia in ratti alimentati con diete specifiche, che in cani diabetici (Zeisel S.H., 2012). In conseguenza a tali ritrovamenti, la colina è ad oggi riconosciuta come un nutriente essenziale per ratti, topi, porcellini d’India, cani, maiali, polli, trote e, più recentemente nel 1998, la US National Accademy of Medicine (accademia nazionale di medicina) ha stabilito i fabbisogni in colina anche per l’uomo. L’apporto di colina si è dimostrato in grado di migliorare lo sviluppo fetale, le funzioni cognitive infantili, l’energia e le performance in atleti, le funzioni cognitive in adulti, oltre che le già citate funzioni a livello epatico.
Nell’NRC del 2001 (“Nutrient Requirements of Dairy Catte” – fabbisogni nutrizionali della bovina da latte), gli autori hanno concluso che: “la definizione di un fabbisogno specifico di colina, sia per vacche in lattazione che per vacche in transizione tra l’ultima fase dell’asciutta e l’inizio della lattazione, necessita ancora di ulteriori prove scientifiche rispetto a quelle disponibili ad oggi”. Da allora, il patrimonio di prove e informazioni relative ai benefici dell’apporto di colina in vacche in transizione è costantemente aumentato.
Il presente articolo si pone l’obiettivo di valutare l’impatto che la supplementazione di colina ha sulla salute delle vacche in transizione.
Nella fase in cui le vacche si avvicinano al parto, esse vanno incontro ad una serie di cambiamenti ormonali in grado di determinare un imponente aumento della mobilizzazione di grassi dal tessuto adiposo. Questo determina una immediata crescita della concentrazione degli acidi grassi non esterificati (NEFA) a livello ematico, che, abbinata ad un afflusso due volte superiore di sangue a livello epatico, risulta in un incremento 13 volte superiore al normale dell’assorbimento di questi complessi lipidici da parte del fegato (Reynolds et al., 2013). I NEFA possono sia essere utilizzati dal fegato come fonte energetica, sia parzialmente ossidati a corpi chetonici, sia veicolati ad altri tessuti in forma di lipoproteine a bassa densità (VLDL) che immagazzianti come grassi negli epatociti (cellule del fegato). La completa ossidazione per produrre energia e la veicolazione in forma di VLDL sono esiti positivi, mentre, un’esagerata parziale ossidazione può risultare nello sviluppo di chetosi. Infine, un eccessivo accumulo di grasso a livello di tessuto può determinare l’insorgenza della steatosi epatica che, a sua volta, ha importanti effetti negativi sulla salute dell’animale.
Bobe et al. (2004), hanno evidenziato come il 50-60% delle vacche in transizione possa andare incontro a steatosi epatica moderata o severa. Le conseguenze metaboliche di un eccessivo accumulo di grasso nel fegato includono ridotte gluconeogenesi, ureagenesi, clearance ormonale e attività ormonale. Gli animali affetti dalla patologia del fegato grasso evidenziano sintomi non specifici di malattia quali: ridotta assunzione di sostanza secca, eccessiva perdita di peso, ridotta produzione di latte, maggiore predisposizione all’insorgenza di infezioni come metriti e mastiti e ad altre patologie metaboliche (ritenzione di placenta, ipocalcemia e dislocazione dell’abomaso), oltre che peggiori performance riproduttive. Non sorprende quindi che la steatosi epatica abbia effetti economici negativi sul rendimento aziendale.
E’ tuttavia fondamentale riconoscere che la mobilizzazione dei grassi in forma di NEFA è essenziale! Tutte le vacche al parto vanno in bilancio energetico negativo e tutte le vacche mobilizzano tessuto adiposo in forma di NEFA. Senza lipomobilizzazione ci sarebbe meno glucosio disponibile per la sintesi di lattosio a livello della ghiandola mammaria e, di conseguenza, minor produzione di latte. La chiave per una corretta transizione e per incrementare la produzione di latte al picco, sta nella capacità di fornire strumenti validi al fegato per gestire in maniera efficace l’aumento di afflusso di NEFA e non nel prevenire la mobilizzazione dei grassi. Esistono strategie nutrizionali e di gestione della mandria atte a mediare il tipico calo in assunzione pre-parto e a minimizzare il bilancio energetico negativo e la mobilizzazione di NEFA, ma queste vanno oltre lo scopo di questo articolo. A prescindere da queste strategie, uno strumento chiaramente efficece nella gestione di queste problematiche è l’apporto di colina rumino protetta (sull’argomento, leggi anche “L’esportazione dei trigliceridi dal fegato e il ruolo della colina“).
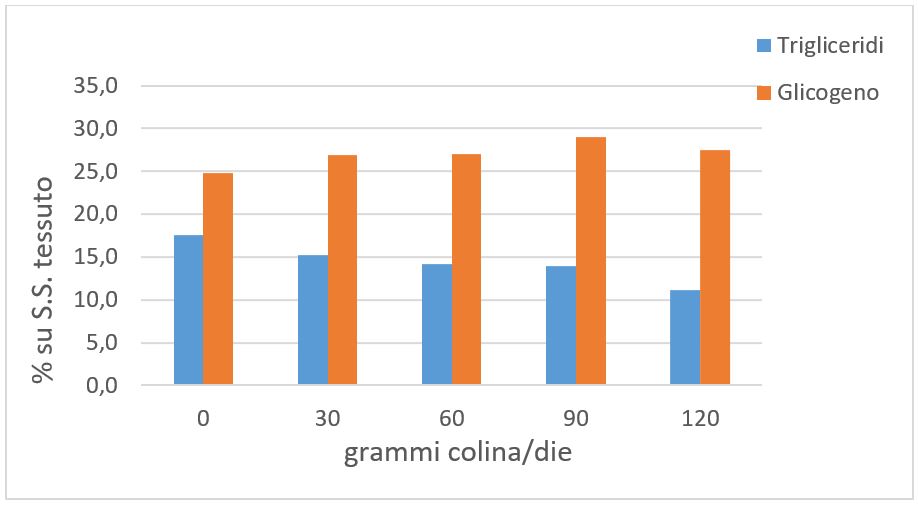
Una delle funzioni principali della colina è di fungere come precursore della fosfatidilcolina, che, a sua volta, è un componente fondamentale per la produzione delle VLDL a livello epatico. Il tasso di produzione delle VLDL (e quindi la capacità di veicolare lipidi al di fuori del fegato) è strettamente connesso a quello di sintesi della fosfatidilcolina (Cole et al., 2011). Il classico sintomo di carenza di colina in molte specie è infatti la patologia del fegato grasso. Non sorprende, quindi, che l’integrazione della dieta di vacche da latte in transizione con colina rumino protetta sia in grado di alleviare il livello di accumulo di grassi nel fegato (Cooke et al., 2007; Zon et al., 2011; Zenobi et al.,2018). La figura 1 illustra i risultati ottenuti dalla somministrazione di incrementali quantitativi di colina rumino protetta (ReaShure, Balchem Corporation) a vacche in asciutta sottoposte a carenza alimentare (Zenobi et al., 2018). Si può notare come all’aumentare dell’apporto di colina, l’accumulo epatico di lipidi diminuisca in maniera lineare e, al contrario, la produzione di glicogeno aumenti.
Figura 1 – Somministrazione di incrementali quantitativi di colina rumino protetta (ReaShure, Balchem Corporation) a vacche in asciutta sottoposte a carenza alimentare ed effetto su accumulo di grassi e produzione di glicogeno a livello epatico.
Nel 2012 Lima et al. hanno condotto due studi su delle grosse stalle commerciali. Nel primo studio sono stati coinvolti 369 animali (primipare e pluripare). La colina rumino protetta (ReaShure, Balchem Corporation) è stata somministrata a partire dai 25 giorni prima del parto fino agli 80 post-parto. La chetosi clinica, le mastiti (casi/vacca), la frequenza di patologie, i trattamenti con destrosio intravenoso e i trattementi con glicole propilenico e calcio propionato per via orale, sono stati tutti significativamente ridotti dal trattamento con colina; inoltre, si è evidenziata una forte tendenza alla riduzione di mastiti. Non è stata evidenziata alcuna interazione tra numero di parto e trattamento.
Nel secondo studio, condotto in vacche primipare, la somministrazione di colina rumino protetta (ReaShure, Balchem Corporation) è stata effettuata esclusivamente per i 22 giorni prima del parto. Gli animali del gruppo trattato hanno evidenziato una frequenza minore di ritenzione della placenta e meno casi di mastiti per animale. Metriti e temperature corporee eccessive al contrario si sono mostrate con maggior frequenza nel gruppo alimentato con colina. E’ tuttavia fondamentale ricordare che gli animali in prova hanno ricevuto colina esclusivamente fino al giorno del parto, e che, quindi, potenziali ulteriori effetti benefici sullo stato di salute in caso di un utilizzo per un periodo prolungato oltre la data di parto, non possono essere valutati.
Più recentemente, Arshad et al. (2020) hanno pubblicato i risultati di una meta-analisi relativa all’integrazione della dieta di vacche da latte in transizione con colina rumino protetta. I risultati hanno evidenziato una tendenza alla riduzione statistica di ritenzione di placenta e mastiti nelle vacche trattate. Oltre a ciò, l’incidenza complessiva di patologie, ad eccezione della chetosi, si è dimostrata numericamente inferiore nelle vacche alimentate con colina.
I costi associati con le patologie metaboliche e le infezioni in vacche in transizione sono estremamente significativi per gli allevatori di bovine da latte. Liang et al. in uno studio del 2017 hanno stimato i costi relativi a 7 comuni patologie metaboliche tipiche in transizione per la realtà produttiva degli Stati Uniti. La Tabella 1 riporta i costi valutati in questo studio, riadattati senza considerare i costi relativi alla mancata produzione di latte e riproporzionati in euro. Infatti, come fortemente supportato nella meta-analisi di Arshad, l’integrazione delle diete in transizione con colina è in grado di determinare un aumento della produzione di latte. Possiamo quindi supporre che parte dell’aumento in produzione di latte sia associabile ad un miglior stato sanitario delle vacche. Quindi, al fine di separare le perdite economiche dovute alla minor produzione dagli altri costi associati alla specifica patologia, i costi realtivi alla mancata produzione di latte sono stati esclusi dal calcolo effettuato nello studio di Liang et al. (2017).
Tabella 1 – Costo totale delle patologie e contributo di ogni singolo elemento (Liang et al., 2017) escludendo il costo per la mancata produzione. Valore in €.
| Trattamenti veterinari | Lavoro | Latte scartato | Aumento giorni aperti | Riforma e morti | Costo totale | |
|---|---|---|---|---|---|---|
| Mastiti | 69.32 | 10.28 | 58.35 | 76.83 | 20.63 | 235.41 |
| Metriti | 80.28 | 8.71 | 36.67 | 75.50 | 23.97 | 225.13 |
| Ritenzioni di placenta | 75.51 | 10.65 | N/A | 75.60 | N/A | 161.77 |
| Dislocazioni | 175.85 | 13.82 | N/A | 76.04 | 54.54 | 320.26 |
| Chetosi | 46.67 | 10.49 | N/A | 76.05 | 11.30 | 144.59 |
| Collasso puerperale | 76.01 | 11.23 | N/A | 76.04 | 49.26 | 212.55 |
Utilizzando l’incidenza e i cambiamenti in frequenza delle patologie presentate nello studio di Lima et al. (2012), possiamo farci un’idea dei potenziali benefici economici dovuti alla integrazione di colina pre e post-parto, relativi al miglioramento dello stato sanitario degli animali e indipendenti dai miglioramenti in produzione di latte (Tabella 2). Queste valutazioni escludono alcuni dati preliminari (Zenobi et al., 2018; Bellotti et al., 2020) che suggeriscono che la colina sia in grado di mitigare la prevalenza dei casi di ipocalcemia subclinica, una delle patologie metaboliche delle vacche in transizione più impattanti a livello economico (non riportato dallo studio di Lima et al., 2012).
Tabella 2 – Potenziale impatto economico della supplementazione con colina durante la fase di transizione – Adattato da Lima et al. (2012).
| Patologia | Incidenza nel gruppo controllo, % | Riduzione nel gruppo trattato, % | Costo della patologia, € | Risparmio su 100 capi |
|---|---|---|---|---|
| Ritenzione di placenta | 11.2 | 9.8 | 161.77 | 177.56 |
| Chetosi cliniche | 11.3 | 65.0 | 144.59 | 1062.01 |
| Dislocazioni | 4.5 | 50.0 | 320.26 | 720.59 |
| Mastiti | 22.5 | 34.2 | 235.41 | 1811.48 |
| Metriti | 11.3 | 29.2 | 225.13 | 742.84 |
| Totale | 4514.48 |
La colina continua ad essere argomento di grande interesse per i ricercatori coinvolti in studi su diverse specie, incluso l’uomo e, come mostrato dai numerosi studi in essere, la vacca da latte. La ricerca effettuata negli ultimi anni ha dimostrato come la supplementazione con colina rumino protetta in vacche in transizione sia in grado di aumentare la produzione di latte durante l’intera lattazione, di migliorare lo stato sanitario degli animali e di ottenere vitelli più sani e più performanti. Molto rimane da capire su come la colina sia in grado di migliorare la salute animale e la ricerca sta continuando a esplorare in questa direzione. Ciò che sembra assolutamente cristallino e che la colina è un alimento essenziale, che diventa limitante durante la fase di transizione quando il fabbisogno diventa elevato e la disponibilità è scarsa.